
大会主题丨坚守质量高地 · 剑指国际化
主办单位丨佰傲谷BioValley
战略合作丨可瑞生物
大会时间丨2022年5月13-14日
大会地点丨中国·北京
大会规模丨1000人

2021年5月28日,国家药监局发布《药品检查管理办法(试行)》,GMP/GSP标准+行政许可,门槛提高了,针对药品生产、经营的飞检频率与力度也在不断增加,“上市许可人”主体责任在逐步强化,可见国家对于药品监管的决心。监管从严的核心在于督促药企建立对自身质量负责的态度和意识,有效的监管与企业的自觉缺一不可,但二者如何相互配合提升药品质量,仍然任重道远。
近年来,在国际形式风波频起、内卷不断、CDE抗肿瘤新政落地等因素下,可谓内忧外患、风雨交加,对于阵痛期的创新药企而言,似乎国际化才是希望的彼岸。时间窗口稍纵即逝,创新药的长期增长更需魄力与毅力。“质量是企业的生命”,药品质量水平的高低决定了其在临床上的表现。2022是创新药国际化元年,当创新出海成为医药最强音,质量人与药政注册人更需修炼内功以应对挑战。
在此背景下,本土药企如何在坚守药品质量标准的前提下,出征海外,是本次大会重点聚焦的话题。由佰傲谷发起主办的2022第三届QbD生物药质量科学大会将于5月13-14日在京隆重召开!本次特设四大平行论坛,召集1000+行业同仁、70+权威大咖与会,共同探索研讨,坚守国内企业药品质量高地、提升质量管理水平,与国际规范同行。
QbD 2022 大会精彩看点不容错过
1.国内第一个:
聚焦生物药质量领域的千人大会
2.连续三年:
药品质量理念和专注态度的延续,兼具深度和广度,全新再出发
3.剑指国际化:
解读创新药国际注册法规和质量要求,理解各国监管文化,制定全球战略
4.云集一流:
顶尖制药巨头、创新型药企、监管部门等的重量级嘉宾
5.理论+实战:
从分析方法研发到质量管理,理论结合实战,提供思路与方法,解决实际问题
参会对象
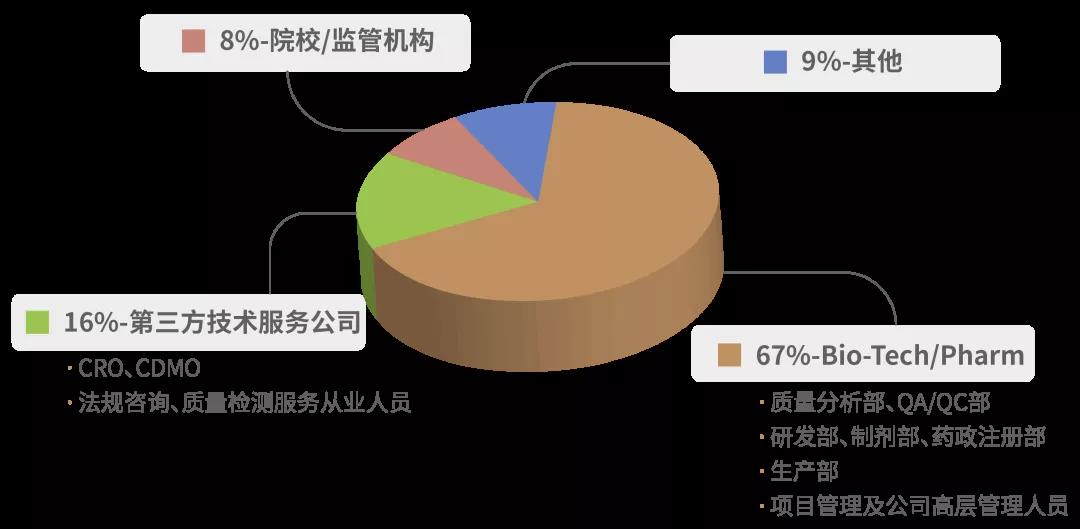
会议日程(最终日程以会议现场为准)
5月13日上午
主论坛
坚守质量高地·剑指国际化
全球主要监管机构药品法规解读和比较
分析方法验证和转移的监管观点
新药研发质量体系建立的关键问题
美国、日本、欧盟、澳洲MAH质量管理实践分享
2020版药典解读
Panel:全球药品注册申报策略和实战经验
欧美中法规关键差异
各国审评官的特点和沟通要点
监管文化的差异
我们离全球同步研发到底有多远
5月13日下午-5月14日全天
论坛一
百抗风云:抗体药物专场论坛
生物大分子药物表征的创新技术
DOE在质量研究方法开发中的应用
HCPs的鉴定方法:旧挑战和最新改进
ADC药物浓度和DAR测定的新平台方法
ADC药物工艺相关杂质和产品相关杂质的质量研究
双特异性抗体关键质量属性的表征方法
FDA对IND申请中生产和质量的要求
创新药质量和稳定性变更的可比性研究和验收标准
双特异性抗体聚集体和颗粒物质的分析和表征策略
论坛二
免疫江湖:细胞与基因专场论坛
基因治疗产品可开发性评估关键检验参数
定量腺相关病毒(AAV)空壳率的CE检测方法
基因治疗产品质量标准制定的关键要点
表征(CAR)T细胞疗法中的残留物的分析策略
制定基因治疗产品分析策略时的监管注意事项
CAR-T 功能检测要点
CAR-T 质量控制体系的建立
细胞疗法产品基于风险评价的微生物污染控制
论坛三
出征海外:全球药品政策法规
中国创新药物在全球范围加快上市的策略与路径
EMA罕病及抗癌药的IND及上市审评要点解读
中美申报IND异同与提交差异
澳洲临床试验申报沟通注意事项和提交流程
MAH关键法规解读和实施要点
监管趋严环境下与CDE高效沟通的策略指导
ADC药物在审评阶段的主要关注点以及注意事项
新的细胞治疗产品如何与监管部门沟通
如何合理规划各模块工作,加快申报节奏
新专利法对生物医药产业的影响
论坛四
新药典·新方法
2020年版《中国药典》三部增修订内容解读
监管科学与药典的协同发展
药典标准|基于SPR技术的双特异性抗体活性检测
质谱技术在蛋白质药物质量研究中的新应用
药典对抗体药物糖基化定量分析的新要求
生物制品生物活性/效价测定方法验证指导原则
外源性DNA残留量测定法
单抗电荷变异体测定法(iCIEF法)
细胞内毒素检查法应用指导原则
现代分析技术在生物药研发及质控中的应用与思考
会议嘉宾(最终出席嘉宾以会议现场为准)
拟邀嘉宾
❖ 百花齐放 · 百家争鸣 ❖
发言嘉宾阵容:
☞ 监管部门:药监局、药检所、药典委、国际审评员、法规起草者
☞ 国际制药巨头
☞ 创新型药企
QbD拟邀嘉宾:
☞ 袁 林 药监局药品监管司司长
☞ 杨昭鹏 国家药典委生物制品处副秘书长
☞ 李国庆 国家药监局法制司 一级巡视员
☞ 王 元 核查中心生物产品检察处 副处长
☞ 余 立 北京市药品检验所 国家局新药评审专家库专家
☞ 王 兰 中检院抗体药物研究室主任
☞ 张伯彦 北京天广实副总经理兼首席科学家
☞ 王董明 信达生物质量高级副总裁
☞ 王 阳 神州细胞副总经理,董事
☞ 王亚君 药明巨诺质量负责人
☞ 李和义 科济生物分析及质量控制副总裁
☞ 蒋燕敏 和铂医药 质量负责人
☞ 孙志刚 绿叶制药集团 质量和监管事务高级副总裁
☞ 张 萍 基石药业质量管理副总
☞ 俞 琦 诺华大中华区质量负责人
☞ Jolanda Westerlaken 优时比全球CMC&Device 负责人
☞ 陈 华 强生公司质量策略亚太总监
☞ Alice Ruan 赛诺菲中国质量部负责人
☞ 周新腾 复星凯特 注册负责人
☞ 邱宇红 传奇生物 全球法规事务副总裁
☞ 闫小军 百济神州 全球药政事务负责人
☞ 许丽锋 康希诺 法规事务部及临床运营中心 高级副总裁
☞ 辛 强 前药明生物 首席质量官
☞ 张 鹏 康方生物 高级副总裁
☞ 黄开胜 荣昌生物 首席质量官
☞ 陶铜静 复星凯特 质量负责人
☞ 吴正宇 诺和诺德 注册事务总监
☞ 马卫东 康宁杰瑞 质量副总裁
☞ 王江华 可瑞生物 CSO
☞ 谭青乔 鼎新生物 CTO
☞ 杜增民 信念医药 工艺开发部总监
☞ 赵忠亮 中吉智药 病毒载体工艺总监
会议门票
2. 标准通票(不包含论坛三:全球药品政策法规专场) 价格:259元/人
- 包含两天会议入场门票(论坛一、二、四)
- 两天豪华商务午餐+会议茶歇
- 会议资料+嘉宾授权ppt
- 前排预留坐席
- 三人及以上享9折团购优惠,4月15日以后注册费用为299元/人
3. 超值尊享通票(包含2022生物制药小编精选汇编本一本)-不包含论坛三:全球药品政策法规专场 价格:359元/人
- 包含两天会议入场门票(论坛一、二、四)
- 两天豪华商务午餐+会议茶歇
- 会议资料+嘉宾授权ppt
- 2022生物制药小编精选汇编一本(市场价:168元/本)
- 前排预留坐席
- 三人及以上享9折团购优惠,4月15日以后注册费为399元/人
4. 论坛三:全球药品政策法规论坛门票-包含大会所有论坛 价格:1600元/人
- 包含两天会议所有论坛入场门票
- 两天超豪华自助午餐+会议茶歇
- 会议资料+嘉宾授权ppt
- 2022生物制药小编精选汇编本一本(市场价:168元/本)
- 前排预留席位
- 团购优惠:3人及以上报名,注册费1400元/人,6人及以上,注册费1200元/人(4月16日前有效)
- 注意:该论坛参会代表仅限200位,售完即止!


